【愛滋新聞】中裕愛滋新藥 向FDA提登記申請
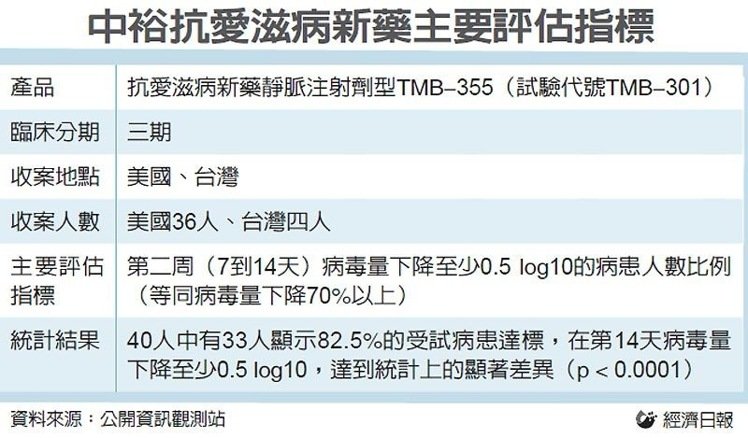
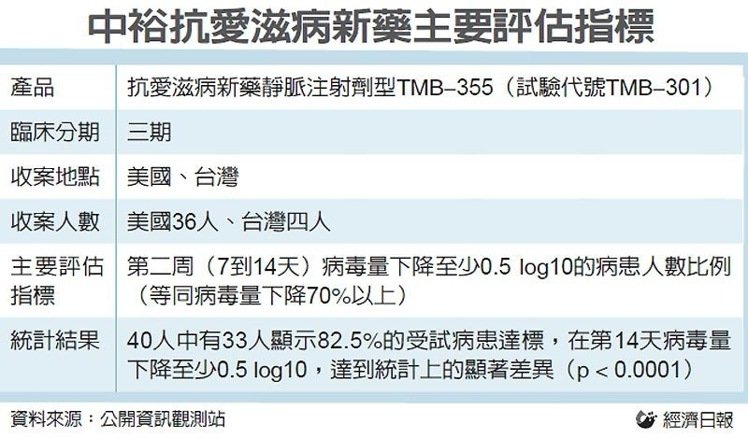
中裕(4147)愛滋病新藥TMB-355今天研發傳喜訊,該公司正式向美國FDA提出生物製劑藥品上市查驗登記申請,法人預估,預計明年第1季將可取得美國藥證並進行銷售,中裕明年有望由虧轉盈。 中裕表示,日前已獲得美國食品藥物管理局(FDA)核准通過研發中之愛滋病新藥TMB-355(ibalizumab)靜脈注射型應用於多重抗藥性病人「突 破性治療資格」(Breakthrough Therapy)。依據突破性治療資格,可以以滾動式方式提出藥證申請及審核,以加速相關作業流程。 中 裕TMB-355是一種治療愛滋病的單株抗體蛋白質藥物,已獨立自主完成生物製劑藥品上市查驗登記申請(BLA)有關藥品生產及測試(CMC)部分,正式以eCTD-submission(電子送件)方式向美國FDA提出藥證審查申請,藉以先行審查該部分資料,以加速未來藥物上市之時程。 中 裕指出,預計要再進行下一階段研發,靜脈注射劑型三期臨床試驗預計在今年10月完成,預計年底前送件提出藥證申 請及審核,因此藥證取得日期約在106年第一季。過程中若開始申請藥證時將會依規定發佈重大訊息。至於肌肉注射劑型後期臨床試驗規劃及範圍,需依據一/二 期臨床試驗結果而定。首次獲得美國FDA藥物核准上市以及未來銷售時才需給付Genentech權利金。 愛滋(HIV/AIDS)藥物全球銷售額約170億美金,市場以歐美為主。僅僅美國銷售金額約90億美金,而絕大部分市場掌握在前五大公司,其中領導廠Gilead產品線多為第1線(初 期)治療用藥,囊括市場超過半數大餅。但愛滋病患者得病多年後,抗藥性開始產生必需開始進入第二線以後之治療用藥,競爭市場就大不相同,主要由默克、必治 妥、ViiV、嬌生等廠商瓜分市場,估計在新藥帶動下,2018年愛滋藥物全球銷售額將成長至180-190億美元。 新聞來源:聯合新聞網 2017/7/20